2022年7月1日,我院徐书华团队与国内多家单位合作在National Science Review发表了题为《Lineage-specific positive selection on ACE2 contributes to the genetic susceptibility of COVID-19》的探究论文。该研究系统性地解析了血管紧张素转化酶2的编码基因ACE2的群体多样性特征,鉴别出在地理人群间差异性分布的ACE2基因谱系,并发现了在东亚人群中尤为显著的谱系特异性自然选择印迹;该研究进一步揭示了ACE2基因谱系与新冠病症轻重程度的统计学关联。
肆虐全球的新冠疫情在不同地域、国家、人群间呈现出有差异的感染风险以及重症率和死亡率。这其中的影响因素固然复杂,包括但不限于地理气候环境、社会生活方式、政府防控政策、医疗卫生条件、个体健康状况等多因素的综合影响。但是在迭代更新的不同病毒株暴露环境下,大量无症状感染者和轻症患者的出现使得个体易感性的差异成为不可忽略的事实。自新冠流行以来,长期争论的一个问题是不同人群以及不同个体间的易感性差异和病症轻重程度是否存在遗传基础,即遗传背景差异或基因多样性是否对易感性起到关键作用?由于目前的共识是新冠病毒利用ACE2基因编码的蛋白作为受体入侵人体细胞,因此有不少研究尝试寻找ACE2基因遗传变异与新冠人群易感性之间的关系,但是尚无研究鉴定出与新冠易感性有关的ACE2基因变异;迄今为止全球开展的全基因组关联分析(GWAS)也并未揭示出ACE2基因变异与新冠易感差异的关联。因此,ACE2基因与新冠易感性之间究竟有何关系依然是一个谜团。
研究团队从群体遗传学角度重新审视ACE2基因在人群中的多样性分布和进化规律,力图阐明基因多样性与新冠易感性之间的内在关联和进化遗传学机制。该研究搜集了覆盖全球210个现存族群6000多人的ACE2基因的全序列数据,以及5000多个古代样本的ACE2基因型数据,系统性地解析了ACE2基因的群体多样性特征,鉴别出在地理人群间差异性分布的ACE2基因谱系,并发现了在东亚人群中尤为显著的谱系特异性自然选择印迹。研究团队进一步与华南理工大学医学院、深圳市第三人民医院、武汉同济医学院、武汉协和医院等合作分析了过千例新冠患者的ACE2基因序列数据,揭示了ACE2基因谱系与新冠病症轻重程度的统计学关联。
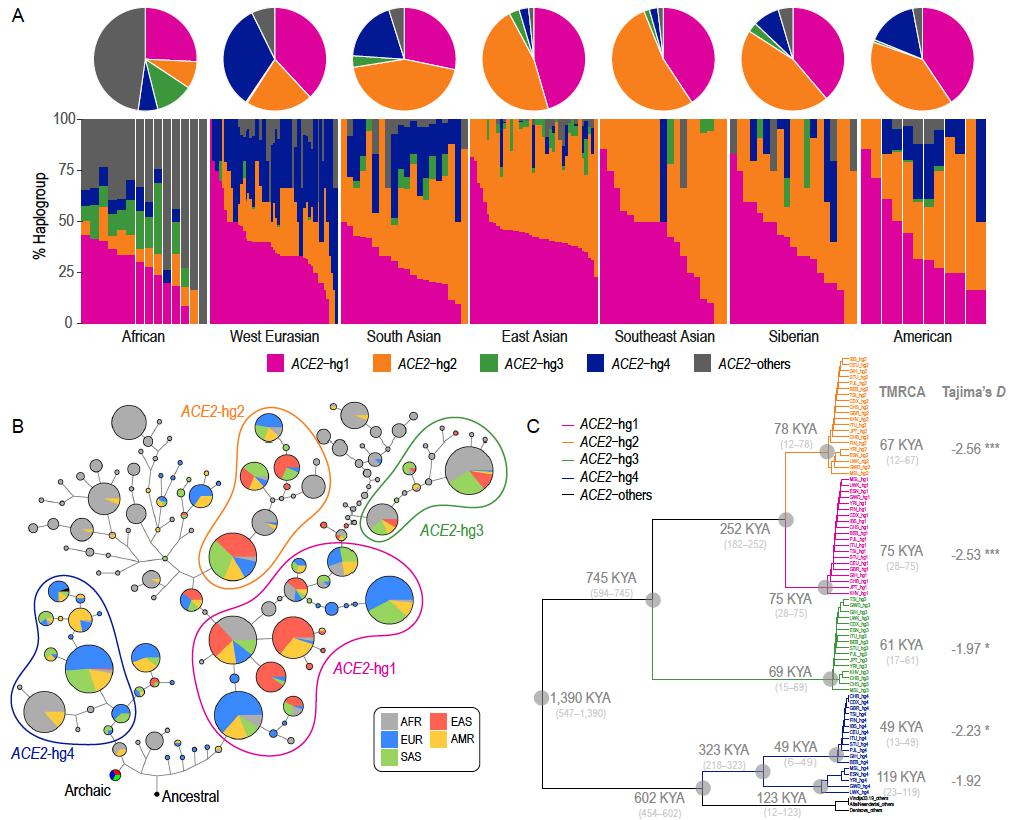
图1: ACE2基因单倍群谱系及ACE2单倍群在全球人群的频率分布
该项研究根据全球人群中的ACE2基因多样性鉴定出4种主要单倍群谱系(hg),即ACE2-hg1(占36% )、ACE2-hg2(占31%)、ACE2-hg3(占6%)、ACE2-hg4(占15%)。4种主要单倍群谱系呈现出人群差异,其中,东亚人群相较其他大洲的人群在ACE2基因上表现出更低的遗传多样性水平——显著低于基因组范围和X染色体范围的预期,主要包含ACE2-hg1与ACE2-hg2两种单倍群谱系,分别占43%和53%(图1)。值得注意的是,ACE2-hg1与新冠重症高度相关,意味着ACE2-hg1携带者具有较高的新冠重症风险;而ACE2-hg2携带者则对应了较低的重症风险(图2)。有趣的是,研究团队发现东亚人群的ACE2-hg2单倍群在史前经历了适应性进化(受到正向自然选择),最初自然选择可能起始于约10万年前,但在距今3千到5千年前达到峰值。目前还很难确定具体的选择压力是什么,但早在新冠疫情之前的病毒感染和大流行可能是其中潜在的驱动力。在包括自然选择在内的进化驱动力作用下,ACE2-hg2最终在东亚人群中达到最高频率,这也导致了东亚人群ACE2基因多样性与其他基因组区域以及其他人群相比都低了很多(图3)。人群历史上经历的这些复杂演化过程最终影响了现存人群内部和人群之间的遗传易感性差异。
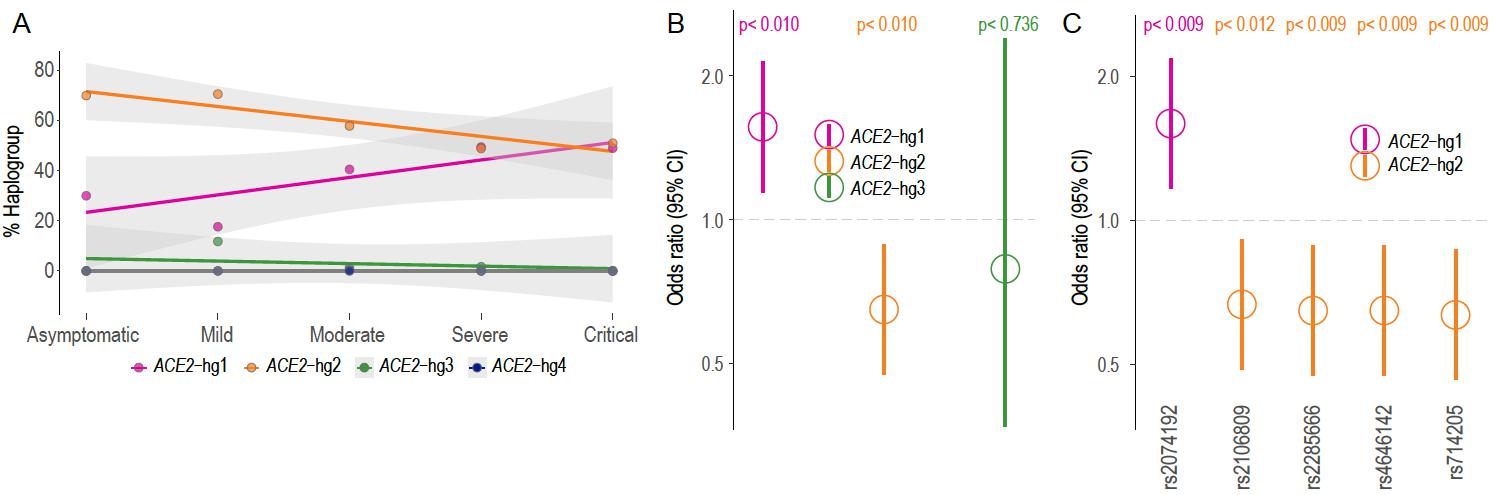
图2:中国汉族新冠患者的ACE2基因单倍群与病症轻重程度的统计关联
该研究首次全面地剖析了ACE2基因在全球人群的多样性与谱系分化以及进化特征,并揭示了早期人群演化历史中形成的ACE2基因多样性对现存人群新冠遗传易感性的影响及机制。研究结果对于理解新冠遗传易感性机制及新冠疫情的防治具有参考意义。然而,需要特别强调的是,尽管该项研究工作表明新冠的易感性在人群和个体间的差异具有遗传基础,但是对每个人来讲最终的结局取决于多方面因素的综合作用。人类基因多样性的形成与人类生活环境中的病毒密不可分,是一个相互作用且具有很大随机性的共进化过程,加之人类社会活动已具有极大不确定性,因而短期内难以做出具有实践意义的预测。因此,人群和个体遗传易感性差异只能作为卫生防疫政策制定的参考依据而非决定因素。
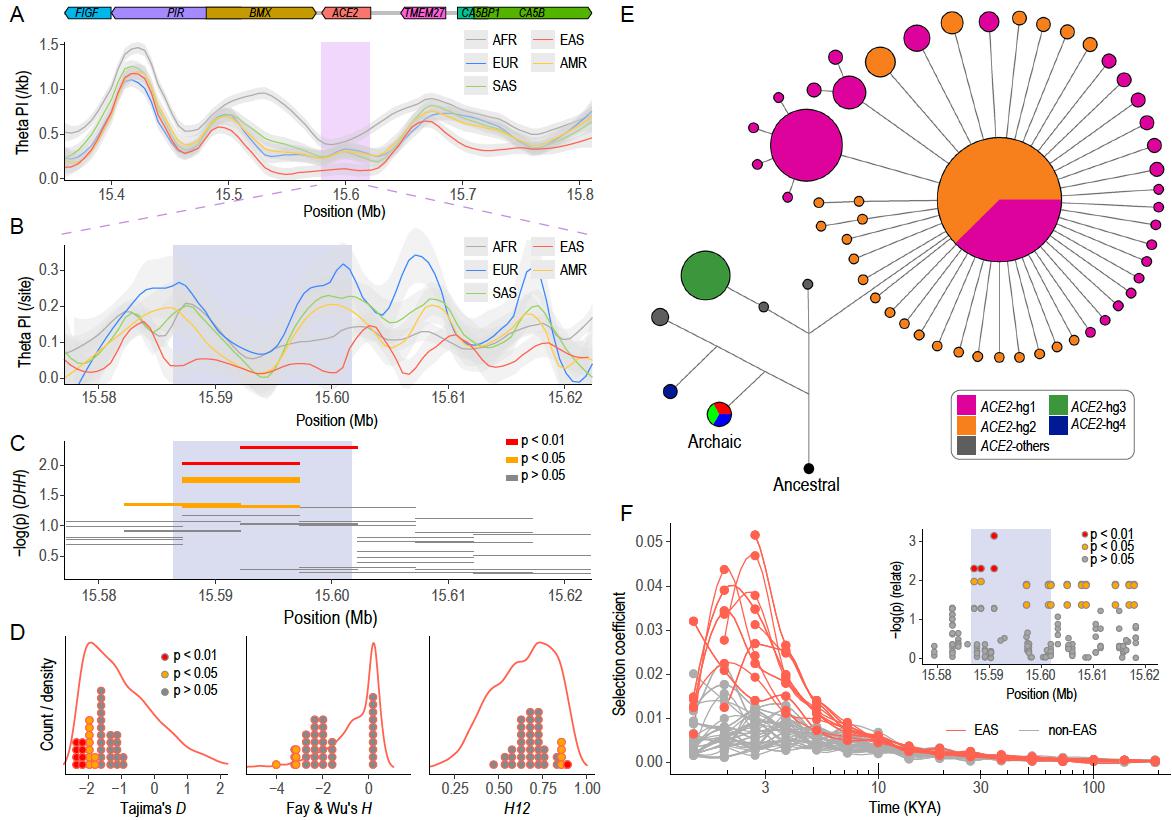
图3:东亚人群ACE2基因多样性与人群早前演化历史中的适应性进化
中国科学院上海营养与健康研究所博士研究生潘雨闻为该论文第一作者,中国科学院大学生命科学院硕士研究生刘盼红为第二作者,复旦大学生命科学学院/附属中山医院徐书华教授为通讯作者。复旦大学生命科学学院、附属中山医院、人类表型组研究院为通讯单位。该项工作与华南理工大学金鑫教授、深圳市第三人民医院王芳教授、武汉同济医学院吴鹏教授、武汉协和医院程范军教授等合作完成。该项工作获得了国家自然科学基金应急专项、中国科学院先导专项、上海市国际人类表型组计划市级科技重大专项等多项基金的资助。
原文链接:https://doi.org/10.1093/nsr/nwac118
