细胞在受到内部或外部刺激后会触发细胞衰老命运,呈现出不可逆的细胞周期阻滞和细胞衰老相关分泌表型等特征。细胞衰老在多种生理病理过程中(如从个体发育到衰老、从伤口愈合到慢性炎症、从抑制肿瘤细胞生长到形成促炎肿瘤微环境)发挥着复杂多样的生物学功能。有效识别衰老细胞成为对其进行操纵并延缓个体衰老和衰老相关疾病的重要前提。尽管一些经典的指标,比如形态学(细胞变大和扁平化)、细胞衰老相关半乳糖苷酶(SA-β-Gal)活性增加以及细胞周期相关的分子标记(如p16、p21),可用于表征细胞衰老,但由于存在细胞衰老的异质性,而且不是所有细胞衰老指标都在各种细胞衰老体系中出现,也没有一个单一指标可以区别所有细胞衰老类型,因此有效鉴定各种条件下的衰老细胞仍存在巨大挑战。
近年来,混合细胞和单细胞转录组技术的飞速发展为基于转录组信息的细胞衰老预测提供了大量数据。一些方法从中提取多个关键基因从而进行基于基因表达权重计算的细胞衰老评分,也有方法利用细胞衰老相关的基因集进行富集评分,还有利用不同机器学习方法开发出的多种细胞衰老评分工具。然而,这些方法大多依赖有限的细胞衰老特征基因或细胞衰老模型,难以较为全面地捕获细胞衰老的共同特征,导致方法的泛化能力不足。此外,这些方法在提取细胞衰老特征时,分别选取了不同细胞类型或不同状态的细胞作为对照组进行差异基因分析或二分类模型训练,未充分考虑负样本(非衰老细胞)的潜在细胞状态等信息的差异对特征提取的影响。因此,开发一个纯粹学习衰老细胞特征而不受各种非衰老细胞特征影响的通用型细胞衰老预测工具,对于衰老研究领域有重要价值。
针对这一需求,2025年5月29日,复旦大学倪挺课题组在Nature Aging期刊上发表了题为A transcriptome-based human universal senescence index (hUSI) robustly predicts cellular senescence under various conditions的研究工作。在该论文中,研究团队创新性地开发出了一个基于转录组数据的人类通用细胞衰老指数(human universal senescence index,hUSI),用于方便和可靠地评估不同条件下混合细胞及单细胞亚群水平的细胞衰老程度。作者系统搜集和标准化处理了来自73项已发表的细胞衰老相关研究中的单一细胞类型转录组测序数据,并通过一系列严格的质控条件,保留了770个衰老和非衰老细胞样本(涵盖34种细胞类型和13种细胞衰老类型),是目前为止最为全面的细胞衰老学习数据集(处理后的数据集可通过访问https://figshare.com/s/0335252fca31a5303510进行下载)。

为了更好地捕获通用的人类细胞衰老特征,作者选取了单分类逻辑回归机器学习算法,该方法不容易受非衰老细胞的类型、状态及混杂信号等因素的影响,从而能够学习到更为纯粹的细胞衰老特征。进而利用基于秩的Spearman相关系数作为预测细胞衰老状态的定量方式,并将其均一化为0到1之间的值,通过比较该值的大小来评估细胞衰老的状态。模型训练过程中,作者通过多项测试证明,与以往的方法相比,该策略在精确性、泛化能力、鲁棒性和生物学可解释性上均表现出色。而在多个独立的混合细胞和单细胞转录组数据集上,hUSI识别衰老细胞的整体精确性均超过了现存的30多种细胞衰老评分方法,并在应用到体内数据集上亦呈现出较好的年龄相关性。作者进一步利用公开数据和实验证明了hUSI计算的细胞衰老得分与经典细胞衰老表型(SA-β-Gal染色变蓝细胞的百分比)的高度相关性。
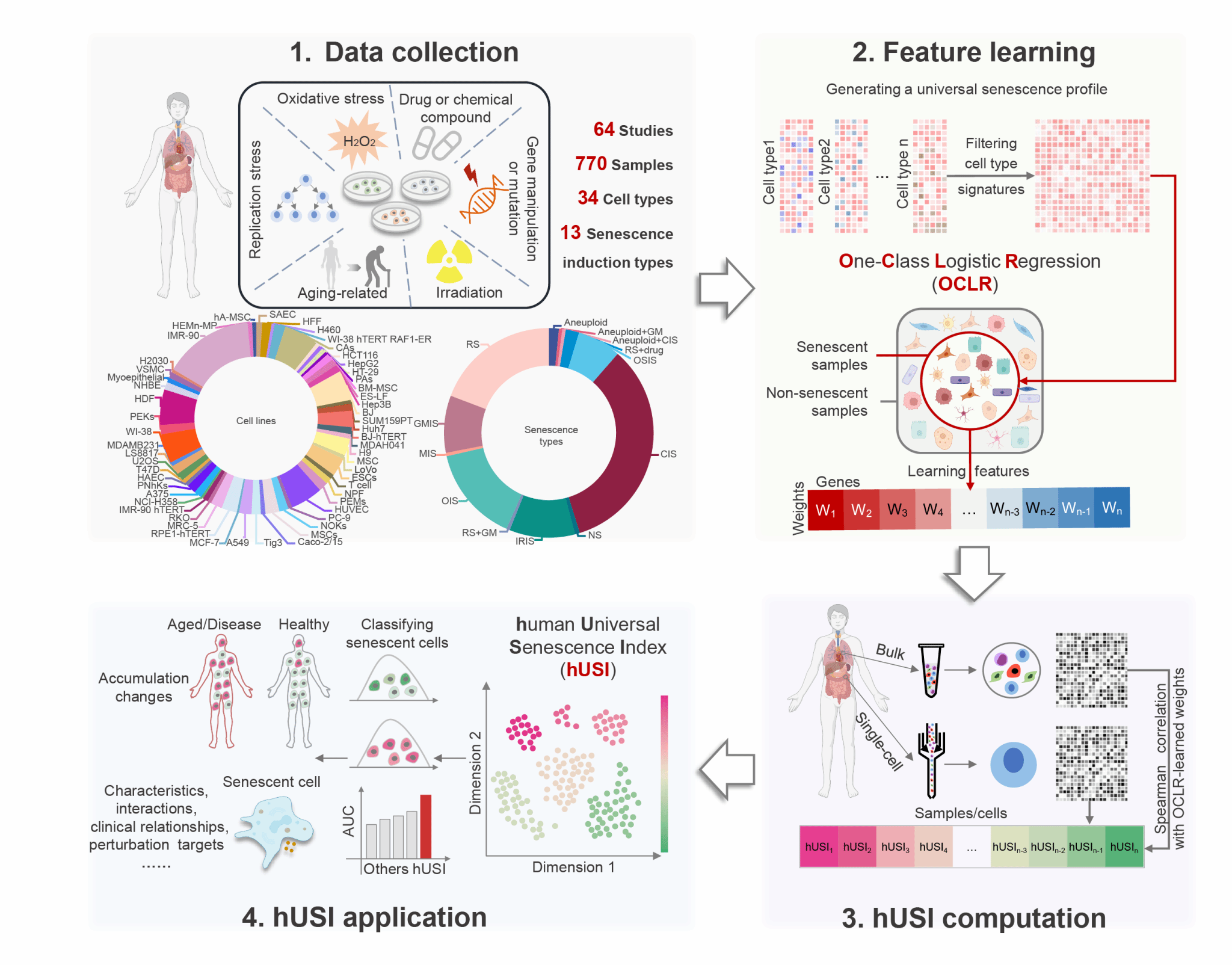
图1. 人类通用型细胞衰老评分工具hUSI的构建及应用示意图
其中hUSI软件包与指导手册已经开源发布(https://github.com/WJPina/HUSI)
进一步,作者将hUSI应用于开放获取的单细胞基因扰动转录组(Perturb-seq)数据,鉴定出了系列潜在的细胞衰老调控基因,敲除这些基因能够显著地增加hUSI评分,并且作者通过实验证明,hUSI鉴定出的前10个候选基因中,有8个基因在敲低后能够显著诱导多种细胞衰老表型,而其中数个基因此前未曾报道与细胞衰老有关。本研究还将hUSI应用到了与细胞衰老密切相关的COVID-19和黑色素瘤的单细胞测序数据中,在前者中揭示了不同细胞类型在病毒感染后细胞衰老水平的变化以及衰老细胞在加重疾病进展方面可能发挥的作用,而在后者中鉴定出了有利于患者生存的衰老肿瘤细胞以及它们在肿瘤微环境中特异的细胞通讯模式。这些研究结果说明了hUSI可助力发现细胞衰老的复杂作用和潜在机制。
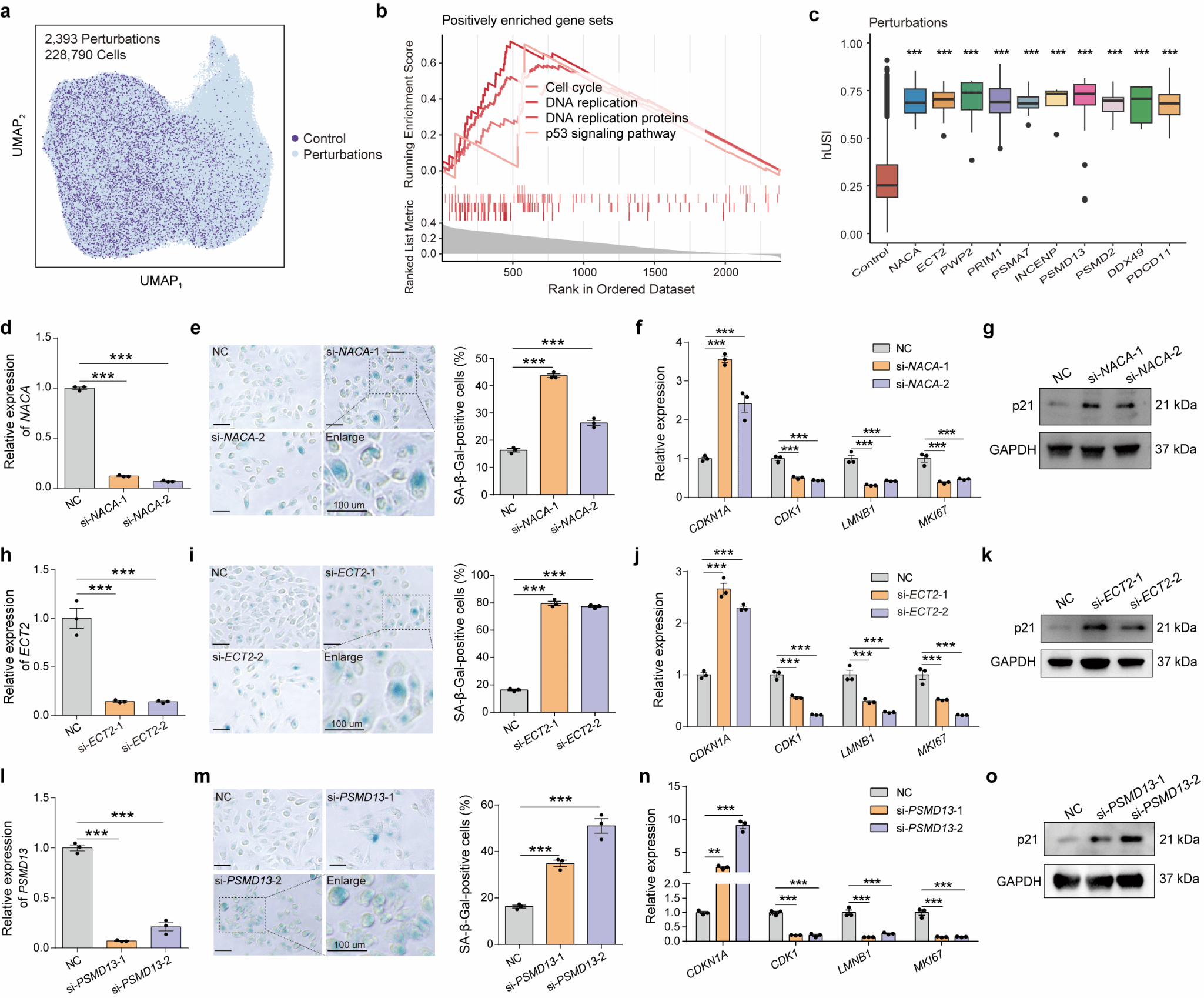
图2. hUSI助力发现细胞衰老调控新基因
综上,该研究开发了兼具鲁棒性和精确性的细胞衰老评估新方法,并利用该方法挖掘出潜在的细胞衰老调控新基因,揭示了不同疾病下衰老细胞的特征和作用,为在大规模单细胞图谱上研究细胞衰老提供了可靠便捷的工具,同时也有望为临床上针对衰老细胞的干预手段提供潜在的参考指标。
复旦大学生命科学学院硕士生王靖、博士生周小兰与余鹏博士后为本论文的共同第一作者,复旦大学生命科学学院/内蒙古大学生物医学研究院倪挺教授为本论文的最后通讯作者,德国慕尼黑亥姆霍兹计算生物研究所的博士生汪伟旭、复旦大学生命科学学院的魏刚博士为本论文的共同通讯作者。内蒙古大学与复旦大学联合培养直博生郭鹏飞和赵宇琪也做了重要贡献。
原文链接:https://www.nature.com/articles/s43587-025-00886-2
